新的膳食成分(NDIs):介绍
按照联邦食品、药物和化妆品法案(使用行为),制造商和分销商希望市场膳食补充剂含有“新膳食成分”必须提交上市前的安全通知(也称为一个NDI通知)向美国食品和药物管理局(FDA)为这些新原料。
新的膳食成分(NDI)需要提交给FDA通知,除非新膳食成分和其他膳食成分出现在膳食补充剂”已经出现在食物供应用于食品的一篇文章的形式食品没有化学变化”(21事项350 b (A) (1))。
FDA NDI指导和过程将探索心脏系列文章之三。在第一部分中,一种膳食成分将被定义,将探索NDI的基础指导,和一些最常见的问题是否需要一个NDI通知将回答。NDI系列的第二篇文章将深入探讨异常通知要求特定的NDIs的历史使用在传统食品和NDI通知提交额外的注意事项。第三、NDI系列的最后一篇文章将提供NDI通知过程的概述,以及需要包括一个NDI通知。最后,NDI通知的决策树,它出现在FDA的指导行业,在最后一篇文章将提供。
定义膳食补充剂和成分
21事项321 (ff)定义了一个“膳食补充剂”任何产品,其他烟草产品,旨在补充饮食和包含“营养成分”。这个定义仅限于可摄取的产品(如片剂、胶囊、粒粉末,液体等)不被认为是一个传统的食品或物品,可以被认为一顿饭或饮食。目前批准的药物或生物制品,或任何药物或生物产品授权进行调查,不属于这一类,除非有问题的产品已经销售作为膳食补充剂之前获得监管部门的批准或授权。
在“膳食补充剂”的定义在321年21事项(ff)(1),一个“营养成分”被描述为:
- 维生素;
- 一种矿物;
- 一个草或其他植物;
- 一种氨基酸;
- 营养物质供人使用来补充饮食增加总膳食摄入量,和/或
- 集中、代谢物、成分、提取物或组合上面描述的任何成分。
简要说明新的膳食成分(NDI)通知
根据FDA的膳食补充剂:新的膳食成分的通知和相关问题:指导工业、NDI通知之前必须提交至少75天产品引入市场。此外,经销商或制造商的新饮食成分或补充提交NDI通知必须为该机构提供的信息已经通知申请人依据他们的结论包含NDI的膳食补充剂将合理预期的安全条件下的推荐或建议使用详细的产品标签。这些信息需要包括任何引用发表的文章。
FDA认为包含NDI的膳食补充剂是掺假如果:
- 所需的上市前的通知不提交给FDA,和/或
- 没有使用的历史或其他证据表明,NDI,当用作推荐或建议在产品标签,合理预计是安全的,即使需要通知已经提交给该机构。
责任制造商/分销商评估膳食成分中使用他们的膳食补充剂产品,确定是否一个NDI提交是十分必要的。如果有不确定性关于膳食成分是否被认为是一种新的饮食成分,一个NDI通知仍有可能提交给FDA。不管提交需求,仍有责任与制造商/分销商,以确保他们的膳食补充剂是安全的,纯粹的。
NDI上市前的通知:所需的信息
- FDA NDI规定指定制造商和/或分销商的信息必须包括在上市前的NDI通知提交(21 CFR 190.6 (b)):
- 制造商或分销商的名称和完整的地址提交NDI通知;
- NDI的名字是上市前的通知的重点
- 如果NDI是植物,其拉丁二项名称必须包括以及科学家的名字给了物质其拉丁二项名称;
- 包含NDI膳食补充剂的描述,包括:
- 水平抗利尿的膳食补充剂,
- 条件补充推荐或建议使用的标签,或者没有条件使用推荐或建议的标签,使用的普通条件的补充;
- 安全使用或其他证据的历史建立膳食成分,使用时在推荐条件下补充规定标签,将预期的安全合理,
- 一个人的签名授权的制造商或经销商代表其签署的通知。
通知要求一个新的膳食成分是什么时候?常见问题的答案
物质不是膳食成分可以NDI吗?
不。密切审查后的描述一个“新的膳食成分”,它变得明显,定义适用于饮食成分没有销售在美国在10月15日之前,1994年。因此,一种物质必须是膳食成分有资格获得新的膳食成分分类。
是一个成分,被用于制造传统食品市场在10月15日之前,1994年,一个NDI吗?
这个问题的答案比之前更复杂的查询,而且,从本质上讲,视情况而定。事实只有一种成分被用于传统食品在10月15日之前,1994年,不确定成分是一种利尿。相反,真正重要的是成分问题是否销售膳食成分在同一时间内。成分一定是销售或膳食补充剂,或用于膳食补充剂,1994年10月15日之前在美国。
简而言之,成分被认为是NDI,除非它也销售作为膳食成分在美国10月15日之前,1994年。
“NDI掺假标准”是什么?
NDI掺假标准提出342年21事项(f) (1) (B)。部分美国法典规定,任何膳食补充剂含有NDI被认为是掺假,除非足够的信息,提供合理保证NDI不构成重大的或不合理的疾病或损伤的风险。
如果一个NDI通知不是必需的,掺假的标准还适用于膳食补充剂含有一个NDI吗?
是的。掺假的标准适用于所有膳食补充剂含有一种抗利尿,即使不需要NDI通知。这是由于这样的事实,只包含补充膳食成分已出现在食品供应中,这些原料被用于食物的形式没有食物的化学改变。
FDA指导的目的是什么时,指的是“营销”膳食成分?
FDA认为接下来的场景来满足“营销”膳食成分的描述。
当一个成分是出售或提供出售:
- 或膳食补充剂;
- 散装膳食成分用于膳食补充剂,或
- 在混合或制定膳食成分用于膳食补充剂。
成分可以挂牌出售:
- 在线;
- 在一个零售机构;
- 在一个目录和价格表,和/或
- 通过广告或其他推广,如果促销很清楚,原料可供购买。
重要的是要注意,“即将推出”的广告不符合或满足FDA的标准“营销”的饮食成分。
如果补充包含NDI出售之前提交一个NDI通知或者小于75天后提交NDI, FDA考虑膳食补充剂或NDI依法出售吗?
/ FDA,产品的销售在这段时间内没有证据表明补充或有人合法销售。
如果膳食成分是美国之外的市场在10月15日之前,1994年,它仍然被认为是一个新的膳食成分(NDI) ?
是的。不能证明的成分不是NDI向FDA提供文档说明成分在其他国家销售在1994年10月的日期之前。唯一的营销是FDA认可和接受有关膳食成分是NDI是否营销之前,发生在美国10月15日,1994年。
哪些文档,FDA建议的例子表明,饮食因素是销售在美国10月15日之前,1994 ?
根据FDA的指导、文档演示膳食成分不是一个NDI应该包括:
- 写业务记录;
- 和/或宣传材料
- 媒体报道的日期10月15日之前,1994年。
这可以包括:
- 销售记录;
- 提单;
- 销售合同;
- 生产记录;
- 商业发票;
- 杂志广告;
- 邮购目录和/或
- 销售手册。
重要的是要记住,文档应该包括足够的信息来建立营销发生在美国。为了证明这一点,营销材料提供给该机构应写明:
- 销售的身份成分(例如化学或植物名称);
- 它的形式(如地面草、水提取物、石油等),和/或
- 原料是否销售的饮食成分或其他目的。
例如,健美杂志上的广告更有可能被认为是足够的证据营销作为膳食成分,而广告或引用一个植物或草药膳食成分在园艺绿化杂志和出版物可能不会营销被认为是足够的证据。
这是大量的信息。有一个快速参考,可以帮助制造商和分销商的膳食补充剂确定膳食成分,事实上,一个NDI吗?
是的。表1提供了一个快速参考指南,可以帮助制造商和分销商的膳食补充剂确定问题是一个抗利尿成分,以及是否需要一个NDI通知,最后,掺假标准是否适用,也总结了常见问题部分。
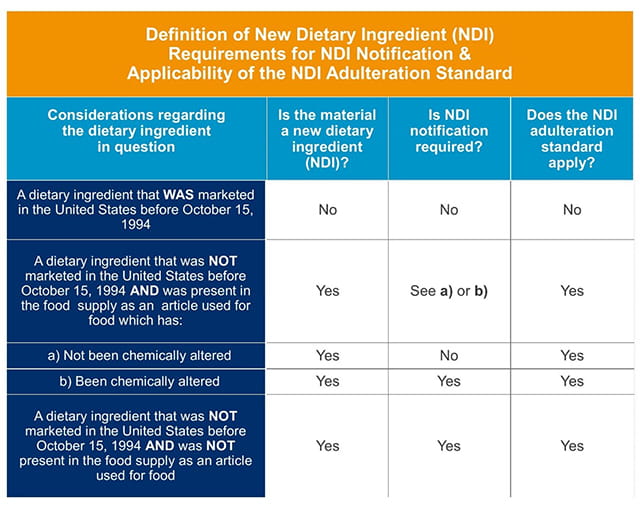
表1。定义新膳食成分,NDI通知要求,NDI掺假的适用性标准
我正在寻找合适的实验室合作。什么服务元素提供膳食补充剂和膳食成分吗万博官网app体育?
万博官网app体育元素有着丰富的经验和专业知识为膳食补充剂提供范围广泛的服务和保健品。我们全面的服务适用于整个产品生命周期,从产品开发到微量污染物和失效分析,认证,稳定,释放和配方优化。作为FDA-registered实验室,我们精通监管意见和咨询专家保持更新最新的监管,行业,和零售商指导、法规和标准。
找到你通过相关文章app1manbetx客户端



