文章
测试方案对医疗器械项目的重要性
在计划任何测试项目时,开发测试协议是至关重要的。了解研究目标和方法将有助于确保成功的测试项目,并降低正在进行和未来的测试项目的风险。方案应明确说明为什么和如何完成测试,需要哪些材料,最重要的是,数据将如何呈现和分析。
我们经常被问到:“我需要一个测试协议吗?”或者“我如何发展一个?”本文档概述了协议的典型部分。在开始任何研究之前,我们强烈建议在开始测试协议,并将与您合作以开发您的测试策略。
为什么有测试计划如此关键?
无论您是在内部执行测试还是将其外包给可信合作伙伴,测试协议都用作捕获期望,验收标准,监管要求和适用标准的主要通信工具,并通过步骤来创建项目计划的步骤。它几乎就像地图。协议还根据将来的重复性作出相应地记录了此信息,并在使用修订控制中将团队保留在同一页面上。不可避免地,随着您从当前职位前进,将来有人会尝试复制您的学习或使用这些信息以备将来的测试目的。具有明确的协议有助于防止未来的不确定性与所做的事情,为什么它已经完成,以及如何进行。
如何开始?
有几个标准部分用于测试协议,根据您的管理策略,您可能希望包含所有协议或根据需要修改它们,以与您的设计历史文件保持一致。其中一些项目可能在其他文件中列出,在两个地方都有可能是多余的。典型的协议部分概述如下:
- 范围
- 目的
- 参考文档
- 测试样品
- 材料和设备
- 方法
- 验收标准
- 异常条件
- 数据分析和文档要求
- 参考文献
修订历史
适当的测试协议需要时间来开发,并且应该在项目的开始分配足够的资源。由于您试图节省时间,所以在项目的中途或事后编写协议常常会导致测试报告中的延迟和不明确的期望。如果制定了正确的步骤,特别是如果您不进行常规测试,那么延迟可以很容易地避免。根据我们的经验,最成功的客户是那些在一开始就预先确定监管需求和风险的客户,然后通过协议来减轻它,而不是匆忙地去做。
FDA发布了指导文档在上市前提交的非临床平台性能测试信息的推荐内容和格式中,可能有助于审查。
范围、背景和目的——目标是什么?为什么?
大多数协议从项目的范围或背景开始。它为设备奠定了基础,以及为什么正在评估它。目标或目的定义了输出。一个明确的目标设置项目的基调,并确定正在回答的问题或正在制定假设。下面列出了几个例子,以增加影响和清晰度:
- 进行测试以评估部分膝关节置换的强度。
- 描述单髁膝关节置换术系统的前后、中外侧和旋转约束行为。
- 该测试涵盖了如何根据在体外环境中特定载荷条件下确定的固有关节设计所描绘的运动来量化单髁膝关节置换约束。该测试的特点是参照ASTM F1223的前后拉伸、中横向剪切和旋转松弛。结果将与谓词进行实质等价比较。
参考文档
我们问新客户的第一个问题是,“您是否有一个希望进行测试的测试标准?”答案通常是肯定的。如果不是,那么可能有一个类似的标准来参考或偏离。该部分应列出任何相关标准,并对任何预期偏差进行评论。FDA指南文件也可以作为参考,因为它们可能概述所需的测试。
测试样品,材料和设备
材料部分应该列出测试所需的所有组件、数量和任何其他相关信息。维护可追溯性以确保对要测试的内容有明确的期望也是必不可少的。
示例表如下所示:

有助于测试样本部分的另一个项目是最糟糕的理由。对于医疗器械行业,确定用于测试的最坏情况配置至关重要。将其在协议中包含在协议中是有帮助的有限元分析万博官网app体育因为这通常是用户或未来团队成员了解为什么选择这种特定设备尺寸的唯一方法。能够理解这些信息有助于快速识别问题或附加风险,并在项目开始时解决它们。
材料部分也包含将要使用的测试设备或仪器。识别负载能力和测试框架的类型可以帮助确保预期负载在校准范围内,并将任何设备的变异性最小化。还可以包括一般的调优参数,以减少任何风险。可以概述fixture和测试环境,尽管它们也可以在Methods部分中列出。
方法
方法或过程部分概述了实际的测试步骤。它们通常与适用的FDA指导文件和ASTM或ISO测试规范保持一致。如果您不确定如何开始此部分,则标准中的程序部分通常是最佳的目标。
方法部分应该概述测试项目的测试参数:
- 样本准备 - 客户特定的装配说明
- 测试配置
- 测试频率
- 目标周期
- 目标负荷数据或负荷选择方法
- 测试环境
- 检查率
- 控制模式(力/位移)
- 比率
- 波形
此部分还应参考任何先前的研究或测试报告以确保可重复性。如果方法部分有几种不同的测试配置,则应为每个测试类型概述上面列出的参数。方法部分的一个关键区域是列出任何特定装配,拆卸或处理信息的轮廓。还应概述测试块或装载方向,拧紧扭矩和流体收集信息。
另一个关键部分是记录任何定制的固定装置或设置说明。通常,测试设置的原理图或夹具的图纸都包括在内,以清楚地说明如何测试设备。这在开发自定义测试方法时尤为重要。
验收标准和例外条件
定义数据、查找和比较的内容都需要文档化。基于之前的测试或谓词测试确定验收标准可以帮助所有相关人员评估生成的数据,并在需要时快速做出调整。它还驱动过程部分,以确保与谓词进行“苹果对苹果”比较。如果您的设备没有可用的谓词,那么明确的接受标准定义是至关重要的。对测试方案的任何例外、变更或修改也应加以注意和说明。
数据分析和文档要求
测试方案计划还应包括贵公司内部报告程序的报告要求。与方法部分相似,ASTM或ISO测试标准概述了测试的通用交付物。但是,如果您还需要原始数据、特定的照片或检查,这些应该在本节中清楚地概述。统计分析信息也应该概述在这里的数据评估。
你计划提交的监管环境也应该被考虑。例如,日本的PMDA与其他监管机构有不同的要求,需要额外的信息和流程图。提前了解这一点将更容易获取必要的数据,并采取主动措施来减少提交风险。
参考文献
参考文献部分应列出任何适当的参考文献,如测试标准,法规指南,以前的测试报告,出版的文献等。本节帮助确定协议中的信息来自何处,以及在何处访问该信息以获得更多详细信息。
修订记录和签名
一旦协议完成,我们建议进行签名和修订控制,以确保所有各方意识到任何变化,并让每个人都在同一页上。研究负责人、本地管理人员和测试实验室的签字是常见的。可以根据需要添加额外的签名。这可以确保多个人都能看到程序。下面显示了一个签名块示例。根据内部进程的不同,一些协议在首页上有签名块,而其他协议在最后有签名块。
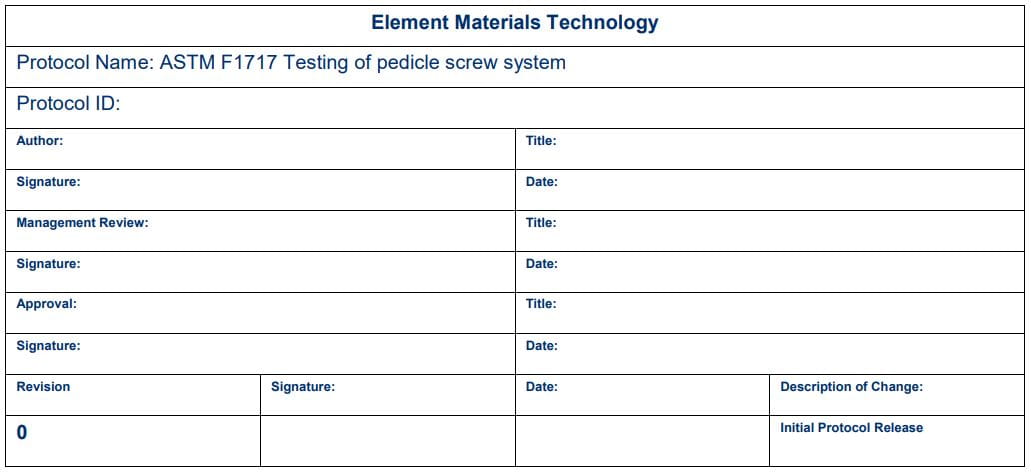
结论
客户经常购买或开发了一定程度的零件,并有机会获得测试程序。测试程序具有实现的测试程序,实现了测试协议以及那些不存在的实质性差异。始终投资协议和测试计划。议定书和计划将减轻您的风险,防止混淆,设置明确的期望,并保留未来参考和使用的必要信息。
万博官网app体育元素是ISO 17025认可,并有一个最广泛的医疗设备测试范围在世界范围整形外科和心血管植入物测试到EMC / EMI /产品安全测试,以及生物和包装评估。联系我们讨论如何帮助您的测试项目。
通过网站找到相关文章核
在近190年的时间里
更多来自元素万博官网app体育

医疗设备
作为一个全面的测试合作伙伴,您将享受单一供应商来源的优势,满足您的所有测试需求,从机械测试和环境模拟到EMC和无线设备测试。
阅读更多

510(k)测试
成功的FDA 510(k)提交对您的市场成功至关重要。不完整或不准确的提交会导致失败,可能会推迟您的产品发布。
阅读更多

医疗器械测试提示
为医疗设备测试程序准备可能对许多制造商来说是一个挑战,特别是如果它是一个新的或新产品,或者时间是有限的。我们的医疗设备专家分享其测试技巧和最佳实践。
阅读更多
注册免费资源
访问Elem万博官网app体育ent的电子邮件订阅中心来接收最新的行业新闻、技术白皮书、案例研究、网络研讨会和即将举行的活动。
阅读更多
